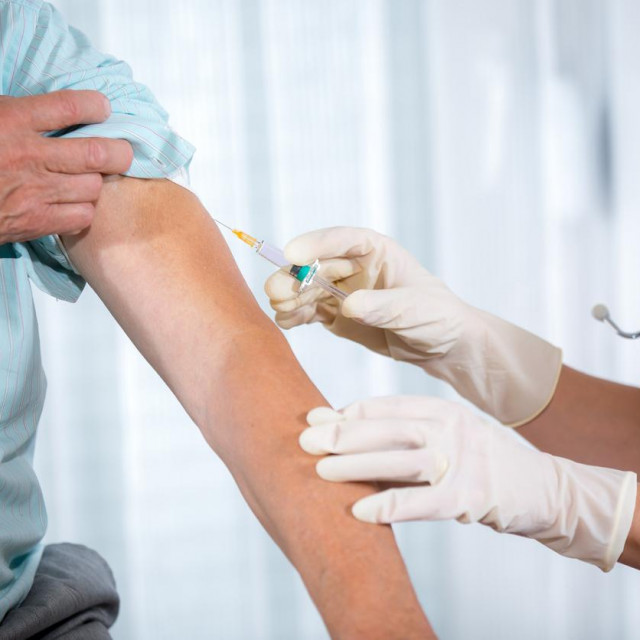
U trećoj fazi kliničkih ispitivanja trenutačno je 12 cjepiva u svijetu. Očekuje se da bi krajem godine mogla biti odobrena dva-tri cjepiva. Neka su cjepiva u Rusiji i Kini već odobrena za ograničenu uporabu.
Kako se provodi treća faza kliničkih ispitivanja?
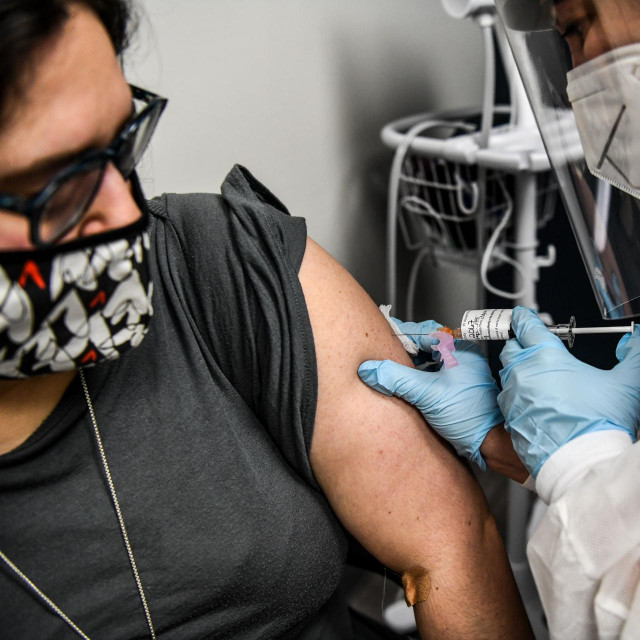
Tijekom treće faze utvrđuje se djelotvornost cjepiva na tisućama dobrovoljaca. Provodi se istodobno u više centara, a često i u više zemalja. To je faza koja prethodi registraciji cjepiva. Kompanije testiraju svoja cjepiva na zdravim dobrovoljcima, pri čemu jedna skupina dobije placebo (inaktivnu tvar koja imitira cjepivo, najčešće fiziološku otopinu), a druga cjepivo.
Na taj način žele utvrditi je li stopa zaraze covidom-19 među onima koji su dobili cjepivo znatno niža nego kod onih koji su primili placebo. Zlatni st...





Za sudjelovanje u komentarima je potrebna prijava, odnosno registracija ako još nemaš korisnički profil....